新教材化学课实验探究课例:铁盐和亚铁盐的一些性质,是我校实施新课程教学中的一个实践。新一轮课程改革对教学设计又提出了更高的要求。《普通高中化学课程标准》(实验)指出:“通过以化学实验为主体的多种探究活动,使学生体验科学研究的过程,激发学习化学的兴趣,强化科学探究的意识,促进学习方式的转变,培养学生的创新精神和实践能力。”因此,在教学中必须强化实验的功能,改变以往的实验只是起演示和辅助的作用,重视化学实验及化学实验教学的设计,以培养学生的化学实践能力、创新精神、科学方法和合作精神。化学教学内容必须加强与社会、生活、生产实际的联系,拓宽学生的视野。教师在教学中要注意开阔思路,综合运用化学及其他学科的知识分析解决有关问题。
一、设计思路
化学新教材中增加了许多探究活动,其中不少活动是探究性的实验。我们对这些探究性的实验要高度重视,要让学生边实验、边探究、边思考、边体验,这对于他们顺利地提出假设,探索现象,验证结果大有裨益。只要教师引导学生亲历探究过程,给学生的自主活动提供机会和空间,就一定能让学生体验到探究活动的乐趣和学习成功的喜悦,并进而体会到化学学习的特点是关注物质的性质、变化、变化过程及其现象等。
本节课通过讨论、发现问题、实验探究、类比等方法让学生自主学习,最终解决以下问题:
1. 用多种方法鉴别铁化合物和亚铁化合物:加碱法和加硫氰化物法
2. 铁化合物和亚铁化合物的相互转化:提供多种氧化剂、还原剂,根据氧化还原基本原理,提出有关铁化合物和亚铁化合物相互转化的条件的假设,学生自主对药品分类、选择药品、设计铁化合物和亚铁化合物相互转化的实验方案,进行实验,并且记录现象,得出结论。重要的是氧化还原反应原理的系统应用。这是本节课的重点。
3. 了解铁与人体健康的科学原理和生活常识。
在设计过程中注意提倡问题式教学,让学生主动参与到学习中去;正确引导,使学生的探究向所需的方向进行。通过这种探究发现式的教学方法使学生能够更容易的接受新知识,并且是潜移默化地接受,同时锻炼了学生的思维想象能力、合作能力以及在科学探索中最为重要的动手能力。做学结合,学以致用,两者相互促进
二、教学过程
[复习]铁的氢氧化物的性质。
[讲解]Fe3+ 、Fe2+与碱反应生成的氢氧化物颜色特征,可以作为检验Fe3+ 、Fe2+的一种方法。下面我们继续研究Fe3+ 、Fe2+的性质。
[科学探究]铁盐和亚铁盐的一些性质
[学生实验探究1]⑴Fe3+离子的检验:取3支试管,试管1 加入4mlFeCl3溶液, 试管2加入4mlFeCl2溶液, 试管3加入FeCl3、FeCl2各2ml混合溶液,观察溶液颜色,再滴入KSCN溶液,观察实验现象并记录。
[教师评价、小结]在Fe2+的溶液2中滴加KSCN溶液无明显现象;在含有Fe3+的溶液1和3中滴加KSCN溶液,溶液变成血红色。
Fe3+的检验: Fe3+ + 3SCN- === Fe(SCN)3 (血红色)
[学生实验探究2](2)Fe3+离子的氧化性:在试管1中,再加入少量铁粉,振荡试管。充分反应后,观察并记录实验现象。再加入几滴氯水,观察实验现象并记录。
[教师评价和小结]试管1中加入少量铁粉,溶液红色褪去;再滴入氯水,溶液又变红色。2Fe3+ + Fe == 3Fe2+;2Fe2++Cl2 == 2Fe3+ + 2Cl-
[思考]如何除去FeCl3溶液中的FeCl2?如何除去FeCl2溶液中的FeCl3?
[学习小组讨论]通过对Fe2+与Fe3+的比较,找出鉴别和检验它们的方法。
[教师评价和小结]:
①加碱法:②加可溶性硫氰化物法:
[学生实验探究3] (3) Fe2+与Fe3+的相互转化:
提供药品:铁粉、铜片、KI溶液、淀粉溶液、CCl4、氯水、酸性高锰酸钾溶液、稀硝酸、双氧水、Vc实验用品:试管、胶头滴管
1. 根据化合价预测可能的氧化、还原性,对药品进行分类。
常见氧化剂
检验试剂
铁粉、铜片、KI溶液、Vc
氯水、酸性高锰酸钾溶液、稀硝酸、双氧水
淀粉溶液、CCl4
2. 利用已有药品用实验验证假设。
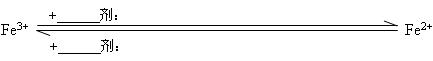
3. 实验探究过程:自主选择相应的药品,设计实验,并开始实验。
预期转化
所选试剂
预期现象
实验现象
结论及反应
→
→
→
→
→
实验探究过程中的问题及解决:
Fe2+ ![]() Fe3+:+强氧化剂
Fe3+:+强氧化剂
Fe3+ ![]()